Thành phần chính của khí thiên nhiên là khí nào trong số các khí sau?
A.\(CO_2\) B.\(H_2\) C.\(CH_4\) D.\(C_2H_2\)
Thành phần chính của khí thiên nhiên là khí nào trong số các khí sau?
A.\(CO_2\) B.\(H_2\) C.\(CH_4\) D.\(C_2H_2\)
Khoanh tròn vào chữ cái đứng trước câu trả lời đúng nhất:
Câu 1: Thành phần chính của khí thiên nhiên là khí nào trong số các khí sau?
A.\(CO_2\) B.\(H_2\) C.\(CH_4\) D.\(C_2H_2\)
Câu 2: Hidrocacbon X cháy trong oxi sinh ra 2 mol \(CO_2\) và 2 mol \(H_2O\). Công thức phân tử của X là:
A.\(CH_4\) B.\(C_2H_6\) C.\(C_2H_4\) D.\(C_4H_{10}\)
Câu 3: Metan và Etilen đều tác dụng với:
A.dd \(NaOH\) B.dd \(Brom\) C.\(Oxi\) D.Rượu etylic
Câu 4: Dãy chất chỉ gồm các hidrocacbon là:
A.\(C_2H_6,CH_3Cl,C_2H_5Br,C_5H_{12}\) B.\(C_4H_8,CH_4,C_2H_6,C_2H_2\)
C.\(C_2H_4O_2,C_4H_8,C_5H_{10},CH_4\) D.\(CH_3Cl,CCl_4,C_2H_6O,C_3H_4\)
Câu 5: Cặp chất đều làm mất màu dd Brom là:
A.Metan,Etilen B.Metan,Axetilen
C.Etilen,Axetilen D.Etilen,Hidro
Câu 6: Để tách metan tinh khiết ra khỏi hỗn hợp gồm metan và etilen, người ta dẫn hỗn hợp sục qua dd nào:
A.dd NaOH dư B.dd Brom dư
C.dd NaCl dư D.nước vôi trong dư
Câu 7: Biết 0,01 mol hidrocacbon X có thể tác dụng tối đa 100ml dd Brom 0,1M. Vậy X là:
A.\(C_2H_2\) B.\(C_2H_4\) C.\(C_2H_6\) D.\(CH_4\)
Câu 8: Biết 0,1 mol hidrocacbon A có thể tác dụng tối đá 100ml dd Brom 2M. Vậy A là:
A.\(C_2H_2\) B.\(C_2H_4\) C.\(C_2H_6\) D.\(CH_4\)
Câu 9: Dãy nào sau đây chỉ chứa hợp chất hữu cơ?
A.\(C_2H_6,Na_2CO_3,CaCO_3\) B.\(C_2H_6,C_2H_4O_2,CH_4\)
C.\(CH_4,CaCO_3,C_2H_4\) D.\(C_2H_4,C_2H_2,Na_2CO_3\)
Câu 10: Nguyên liệu điều chế Axetilen là:
A.Đá vôi B.Vôi sống C.Nước vôi trong D.Canxi cacbua
Câu 11: Phương trình hóa học nào sau đây viết đúng?
A.\(CH_4+2Cl_2\underrightarrow{as}CH_2Cl_2+2HCl\) B.\(CH_4+Cl_2\underrightarrow{as}CH_3Cl+HCl\)
C.\(CH_4+Cl_2\underrightarrow{as}CH_3+HCl\) D.\(CH_4+Cl_2\underrightarrow{as}CH_3Cl+H_2\)
Câu 12: Nguyên liệu điều chế Axetilen là:
A.Đá vôi B.Vôi sống C.Vôi tôi D.Canxi cacbua
Câu 13: Hợp chất hữu cơ là chất khí ít tan trong nước, tham gia phản ứng thế, không tham gia phản ứng cộng. Hợp chất đó là:
A.Metan B.Etilen C.Axetilen D.Propen \(\left(C_3H_6\right)\)
Câu 14: Phản ứng ............. là phản ứng đặc trừng của các phân tử có liên kết đôi, liên kết ba:
A.Thế B.Cộng C.Phân hủy D.Cháy
Câu 15: Cho các hợp chất sau: \(C_2H_2,CO_2,C_2H_4O_2,BaCO_3,NaHCO_3,C_2H_6O,\)
\(C_6H_5Br\) trong đó có:
A.3 hợp chất hữu cơ B.4 hợp chất hữu cơ
C.5 hợp chất hữu cơ D.6 hợp chất hữu cơ
Câu 16: Trong các loại nhiên liệu sau, nhiên liệu nào khi cháy ít gây ô nhiễm môi trường nhất:
A.Nhiên liệu khí B.Nhiên liệu lỏng
C.Nhiên liệu rắn D.Tất cả các loại nhiên liệu trên
Câu 17: Đốt cháy hoàn toàn m g hidrocacbon A thu được 2,24 1 \(CO_2\) (đktc) và 1,8g \(H_2O\). Giá trị m là:
A.14 gam B.1,4 gam C.12 gam D.1,2 gam
Câu 18: Công thức cấu tạo nào sau đây viết đúng?
H H H H H H
↑ ↑ ↑ ↑ ↑ ↑
A.H ← C → H B.H ← C ↔ O → H C.H ← C ↔ C→ H D.H ← C = C → Br
↓ ↓ ↓ ↓↓ ↓ ↓
H H H HH H H
Khi đốt 1,12 lít khí thiên nhiên chứ CH4, N2, CO2 cần 2,128 lít O2. Các thể tích khí đo ở cùng điều kiện. Phần trăm thể tích của CH4 trong khí thiên nhiên là?
\(CH_4+2O_2\rightarrow CO_2+2H_2O\\ n_{CH_4}=\dfrac{1}{2}n_{O_2}=\dfrac{1}{2}.\dfrac{2,128}{22,4}=0,0475\left(mol\right)\\ \%V_{CH_4}=\dfrac{0,0475.22,4}{1,12}.100=95\%\)
một loại khí thiên nhiên có thành phần phần trăm về thể tích các khí như sau 85%(CH4), 10% (C2H6), 2% (nito)và 3 % (CO2) . tính số mol ko khí dùng để đốt cháy hết 1 mol khí trên bt khí Oxi chiếm 20 thể tích ko khí và các khí đo cùng ở điều kiện về nhiệt độ và áp suất
1. Trong 1000 m 3 khí thiên nhiên có 850 m 3 C H 4
2 C H 4 → 1500 ° C C 2 H 2 + 3 H 2
CH ≡ CH + HCl → 150 - 200 ° C , H g C l 2 C H 2 = C H - C l
Khối lượng vinyl clorua thu được (nếu hiệu suất các quá trình là 100%) là:
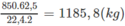
Với hiệu suất cho ở đầu bài, khối lượng vinyl clorua là:
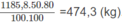
2. Nhiệt lượng cần dùng để làm nóng 100 lít nước từ 20 ° C lên 100 ° C :
100.4,18.(100 - 20) = 33440 (kJ)
Vì 20% nhiệt lượng đã toả ra môi trường nên nhiệt lượng mà khí thiên nhiên cần cung cấp phải là :
Đặt số mol C 2 H 6 tà x thì số mol C H 4 là 85. 10 - 1 x.
Ta có 1560x + 88085. 10 - 1 x = 41800
x = 462. 10 - 2
Thể tích khí thiên nhiên cần dùng:
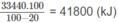
1.Trong phòng thí nghiệm, khí X được điều chế và thu vào bình tam giác như hình vẽ bên (Hình 1.1):
a. Hình 1.1 mô tả cách thu khí X bằng phương pháp nào?
b. Khí X có thể là khí nào trong các khí sau: H2, Cl2, O2, NH3, CH4, SO2, CO2, HCl, H2S, C2H4? Giải thích?Hỗn hợp X gồm: Mg (0,10 mol), Al (0,04 mol) và 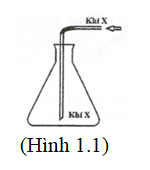
2. Hỗn hợp X gồm: Mg (0,10 mol), Al (0,04 mol) và Fe (0,15 mol). Cho X tác dụng với dung dịch H2SO4 loãng (dư), sau khi các phản ứng xảy ra hoàn toàn thấy có a (mol) H2SO4 đã tham gia phản ứng và khối lượng dung dịch tăng m gam.
a. Viết phương trình hóa học của các phản ứng xảy ra.
b. Tính a và m.
thu khí X bằng cách đẩy KK
vì thu khí bằng cách đặt ngửa bình nên khí X nặng hơn KK
nên khí X có thể là -Cl2 : M=71 g/mol
-O2 : M = 32 g/mol
- SO2 : M = 64 g/mol
- CO2 : M = 44 g/mol
- HCl : M = 36,5 g/mol
- H2S : M = 34 g/mol
M.n giải giúp e với ạ!!
Một loại khí thiên nhiên có thành phần phần trăm về thể tích các khí như sau 85%(CH4), 10% (C2H6), 2% (nito)và 3 % (CO2) . tính số mol ko khí dùng để đốt cháy hết 1 mol khí trên bt khí Oxi chiếm 20% thể tích không khí và các khí đo cùng ở điều kiện về nhiệt độ và áp suất
n CH4 = 1.85% = 0,85(mol)
n C2H6 = 1.10% = 0,1(mol)
$CH_4 + 2O_2 \xrightarrow{t^o} CO_2 + 2H_2O$
$C_2H_6 + \dfrac{7}{2} O_2 \xrightarrow{t^o} 2CO_2 + 3H_2O$
Theo PTHH :
n O2 = 2n CH4 + 7/2 n C2H6 = 2,05(mol)
n không khí = n O2 : 20% = 2,05 : 20% = 10,25(mol)
Khí thiên nhiên được dùng làm nhiên liệu và nguyên liệu cho các nhà máy sản xuất điện, sứ, đạm, ancol metylic,… Thành phần chính của khí thiên nhiên là
A. Metan
B. Etilen
C. Etan
D. Axetilen
Một loại khí thiên nhiên có thành phần về thể tích như sau:
85% C H 4 ; 10% C 2 H 6 ; 3% N 2 ; 2% C O 2 .
1. Người ta chuyển metan trong 1000 m 3 (đktc) khí thiên nhiên đó thành axetilen (hiệu suất 50%) rồi thành vinyl clorua (hiệu suất 80%). Viết phương trình hoá học của các phản ứng và tính khối lượng vinyl clorua thu được.
2. Người ta đốt cháy hoàn toàn khí thiên nhiên đó để đun nóng 100 lít nước từ 20 ° C lên 100 ° C . Tính thể tích khí thiên nhiên (đktc) cần đốt, biết rằng nhiệt lượng toả ra khi đốt cháy 1 mol CH4 và 1 mol C 2 H 6 lần lượt là 880 kJ và 1560 kJ ; để làm cho lml nước tăng thêm 1 ° cần 4,18 J và khi đốt khí thiên nhiên, 20% nhiệt lượng toả ra môi trường không khí.
1. Trong 1000 m 3 khí thiên nhiên có 850 m 3 C H 4
2 C H 4 → 1500 ° C C 2 H 2 + 3 H 2
CH ≡ CH + HCl → 150 - 200 ° C , H g C l 2 C H 2 = C H - C l
Khối lượng vinyl clorua thu được (nếu hiệu suất các quá trình là 100%) là:
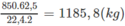
Với hiệu suất cho ở đầu bài, khối lượng vinyl clorua là:
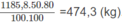
2. Nhiệt lượng cần dùng để làm nóng 100 lít nước từ 20 ° C lên 100 ° C :
100.4,18.(100 - 20) = 33440 (kJ)
Vì 20% nhiệt lượng đã toả ra môi trường nên nhiệt lượng mà khí thiên nhiên cần cung cấp phải là :
Đặt số mol C 2 H 6 tà x thì số mol C H 4 là 85. 10 - 1 x.
Ta có 1560x + 88085. 10 - 1 x = 41800
x = 462. 10 - 2
Thể tích khí thiên nhiên cần dùng:
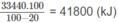
Trong công nghiệp polietilen (PE) được điều chế từ metan theo sơ đồ
C H 4 → H 2 - 80 % C 2 H 2 → H 2 - 80 % C 2 H 4 → H 2 - 80 % P E
Để tổng hợp 5,376 kg PE theo sơ đồ trên cần V m3 khí thiên nhiên (đktc, chứa 75% metan theo thể tích). Giá trị của V là
A. 11,2
B. 22,4
C. 28,0
D. 16,8
Trong công nghiệp polietilen (PE) được điều chế từ metan theo sơ đồ:
C H 4 → H 2 = 80 % C 2 H 2 → H 2 = 80 % C 2 H 4 → H 2 = 80 % P E
Để tổng hợp 5,376 kg PE theo sơ đồ trên cần V m 3 khí thiên nhiên (đktc, chứa 75% metan theo thể tích). Giá trị của V là
A. 11,2
B. 22,4
C. 28,0
D. 16,8